|
Por Sebastián García-Restrepo Fundación Proyecto Primates Consejo Directivo APC s.garciar@uniandes.edu.co
Un año más tarde, Wallace y Bates, deciden separarse para trabajar de manera independiente. Wallace pasaría varios años explorando el Río Negro, recolectando especímenes y tomando notas sobre las poblaciones humanas y sus lenguas, la geografía, la flora y la fauna. Finalmente, el 12 de julio de 1852, se embarca en el Helen para su regreso a Inglaterra, aunque tres semanas después el barco de vapor se incendió ocasionando la pérdida de la gran mayoría de las colecciones que transportaba (Wallace, 1852a; Fonfría-Díaz, 2014). Posterior a la expedición, uno de sus primeros artículos científicos fue “On the monkeys of the Amazon” donde describe al “gran valle del Amazonas” como una región rica en primates, reportando haber visto personalmente 21 especies donde se incluyen aulladores, monos araña, churucos, maiceros, uakarís, micos voladores, monos nocturnos y titíes. El aporte más importante de esta obra es que describe por primera vez la existencia de límites geográficos en la distribución de especies (Wallace, 1852b). Algunas de las preguntas que se plantea en este momento son ¿Qué características físicas determinan los límites de las especies y los géneros? y ¿Cuáles son las circunstancias que permiten a ciertos ríos y ciertas montañas establecer límites para algunas especies y para otras no? En la última página Wallace indica haber encontrado que el río Negro, el Amazonas y Madeira formaban límites que ciertas especies no podían traspasar. Menciona también que los cazadores conocían perfectamente este hecho y cruzaban el río cuando querían conseguir determinados animales que se encontraban solo en la orilla de un lado del río, pero nunca en el otro (Wallace, 1852b). En la actualidad, se conoce que muchos ríos son barreras físicas para la dispersión de animales terrestres y arbóreos que, al menos en la Amazonía, corresponden a los límites de distribución de muchos grupos de especies hermanas. Respecto a esto, la hipótesis de la barrera riberina (Riverine Barrier Hypothesis) confiere un rol principal a los grandes ríos, dado que actúan como barreras para el flujo genético ocasionando que las poblaciones que se encuentran aisladas sobre márgenes opuestos puedan divergir gradualmente hasta formar linajes separados. Alternativamente, los ríos pueden servir como barreras para el contacto secundario entre poblaciones previamente aisladas y en proceso de expansión geográfica (Moritz et al., 2000; Vences et al., 2009). La hipótesis incluye las siguientes predicciones*:
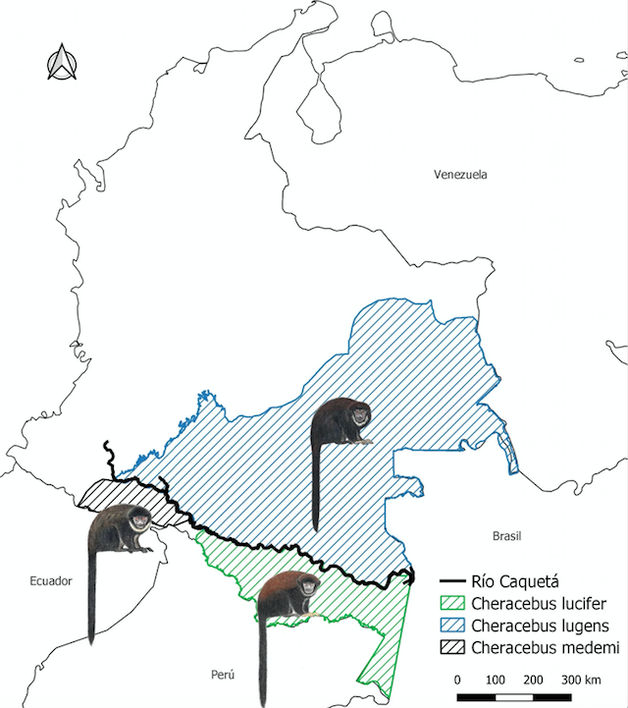
En lo correspondiente a estudios del orden Primates, se ha encontrado que la distribución de algunos grupos parece estar limitada por grandes ríos (Sudamérica: Wallace, 1852; Ayres y Clutton-Brock, 1992; Boubli et al., 2015; Lynch-Alfaro et al., 2015; Merces et al., 2015. Madagascar: Goodman y Ganzhorn, 2004. África: Grubb, 1990; Harcourt y Wood, 2012) y que para ciertas especies, éstos se correlacionan con su diferenciación genética. Este es el caso de los orangutanes (Pongo pygmaeus) a través del río Kinabatangan en Sabah, Borneo (Arora et al., 2010; Goossens et al., 2005; Jalil et al., 2008); chimpancés (Pan troglodytes) en el río Sanaga en Camerún (Gonder et al., 2006); bonobos (Pan paniscus) en la República Democrática del Congo (Erikssonn et al., 2004) y lémures en Madagascar (Markolf y Kappeler, 2013; Olivieri et al., 2007; Quemere et al., 2010). Figura 2. Hipótesis de distribución del género Cheracebus en Colombia. Se observa cómo el río Caquetá representa el límite en la distribución de las especies y separa a C. lugens al norte, con C. lucifer y C. medemi al sur. -Mapa elaborado por el autor. Ilustraciones por Stephen D. Nash- En cuanto a algunas de las investigaciones en el neotrópico mencionadas previamente, Boubli et al. (2015) reportan que el río Branco ha sido una importante barrera geográfica limitando la distribución de seis géneros: Cacajao, Callicebus y Cebus al oeste y Pithecia, Saguinus y Sapajus al este. Por su parte, Lynch-Alfaro et al. (2015) y Mercês et al. (2015) comprobaron que el río Amazonas fue una barrera fundamental para la dispersión del género Saimiri durante su historia evolutiva. En Colombia, un caso interesante que ilustra lo propuesto por la hipótesis de los ríos como barreras es la distribución de las especies del género Cheracebus. El arreglo taxonómico vigente, propuesto por Byrne et al. (2016), reconoce seis especies, de las cuales tres ocurren en Colombia. En la Figura 2 se observa cómo el río Caquetá tiene un papel importante en la distribución de C. lucifer, C. lugens y C. medemi, de acuerdo con los modelos elaborados en el proyecto Modelos de distribución de Primates en Colombia (García-Villalba et al., 2017; Moreno et al., 2017a; Moreno et al., 2017b). Disponibles en: www.asoprimatologicacolombiana.org/modelos-de-distribucion.html A pesar de que el ejemplo anterior es un sistema de estudio interesante para poner a prueba la hipótesis, no se conocen estudios genéticos que busquen una aproximación al respecto. Quizás, el único río que se ha evaluado recientemente como promotor de divergencia en Colombia es el río Magdalena. Sin embargo, aunque este río es una de las barreras geográficas y ecológicas más importantes en los valles inter-andinos del norte de Suramérica, su rol como barrera para el flujo genético ha sido evaluado en pocos estudios (Haffer, 1967; Link et al., 2015; Muñoz‐Ortiz et al., 2015; Sandoval et al., 2017). Investigaciones como las de Link et al. (2015) no encontraron evidencia de estructuración genética en poblaciones de Ateles hybridus que ocupan bancos opuestos del río Magdalena, lo que en otras palabras indica que el río no ha sido una barrera infranqueable para el flujo genético. Este resultado es acorde con lo obtenido por Sandoval et al. (2017) con cuatro especies de aves muestreadas a lo largo del río, pero difiere de Muñoz-Ortiz et al. (2015) quienes reportan el efecto del río como barrera en ranas del género Rheobates. Para terminar, cabe resaltar que actualmente la Fundación Proyecto Primates y el Laboratorio de Ecología de Bosques Tropicales y Primatología, adelantan investigaciones utilizando marcadores mitocondriales y microsatélites para entender los efectos de algunos ríos sobre la estructura genética de primates en la región del Magdalena Medio. Aun así, son necesarios más esfuerzos y colaboraciones institucionales para generar mejores aproximaciones al conocimiento en este campo poco explorado en el país. * Capparella, 1988; Capparella, 1991; Ayres y Clutton-Brock, 1992; Peres et al., 1996; Gascon et al., 1998; Gehring et al., 2012. Agradecimientos A Stephen D. Nash por compartir y permitir el uso de sus ilustraciones. Referencias
Arora, N., Nater, A., van Schaik, C.P., Willems, E.P., van Noordwijk, M.A., Goossens, B., Morf, N., Bastian, M., Knott, C. y Morrogh-Bernard, H. (2010). Effects of Pleistocene glaciations and rivers on the population structure of Bornean orangutans (Pongo pygmaeus). Proceedings of the National Academy of Sciences, 107(50), 21376-21381. Ayres, J.M. y Clutton-Brock, T.H. (1992). River boundaries and species range size in Amazonian primates. The American Naturalist, 140(3), 531-537 Boubli, J.P., Ribas, C., Lynch-Alfaro, J.W., Alfaro, M.E., Nazareth, M., da Silva, F., Oihno, G.M., y Farias, I.P. (2015). Spatial and temporal patterns of diversification on the Amazon: A test of the riverine hypothesis for all diurnal primates of Rio Negro and Rio Branco in Brazil. Molecular Phylogenetics and Evolution, 82, 400–412 Byrne, H., Rylands, A.B., Carneiro, J.C., Lynch Alfaro, J.W., Bertuol, F., Da Silva, M.N., Messias, M., Groves, C., Mittermeier, R.A., Farias, I., Hrbek, T., Schneider, H., Sampaio, I., y Boubli, J.P. (2016). Phylogenetic relationships of the New World titi monkeys (Callicebus): first appraisal of taxonomy based on molecular evidence. Frontiers in Zoology, 13(1), 10. Capparella, AP. (1988). Genetic variation in Neotropical birds: implications for the speciation process. Acta Congressus Internationalis Ornithologici, 19, 1658-1673. Capparella, A.P. (1991). Neotropical avian diversity and riverine barriers. Acta Congressus Internationalis Ornithologici 20, 307-316. Erikssonn, J., Gottfried, H., Christophe, B. y Linda, V. (2004). Rivers influence the population genetic structure of bonobos (Pan paniscus). Molecular Ecology, 13(11), 3425-3435. Fonfría-Díaz, J. (2014). Alfred Russel Wallace: Hacia la resolución del problema de las especies. Boletín de la Sociedad Entomológica Aragonesa, 54, 5–34. García-Villalba, J.E., Guzmán-Caro, D.C., et al. Mapa de Cheracebus medemi. (2017). En: http://biomodelos.humboldt.org.co/species/visor?species_id=7024. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt. Gascon, C., Stephen, C.L. y James, P.B. (1998). Patterns of genetic population differentiation in four species of Amazonian frogs: a test of the riverine barrier hypothesis. Biotropica, 30(1), 104-119. Gehring, P.S., Pabijan, M., Randrianirina, J.E, Glaw, F. y Vences, M. (2012). The influence of riverine barriers on phylogeographic patterns of Malagasy reed frogs (Heterixalus). Molecular phylogenetics and evolution, 64(3), 618-632. Gonder, M.K., Disotell, T.R. y Oates, J.F. (2006). New genetic evidence on the evolution of chimpanzee populations and implications for taxonomy. International Journal of Primatology, 27(4), 1103 Goodman, S.M. y Ganzhorn, J.U. (2004). Biogeography of lemurs in the humid forests of Madagascar: The role of elevational distribution and rivers. Journal of Biogeography, 31, 47–55. Goossens, B, Chikhi, L., Jalil, M.F., Ancrenaz, M., Lackman-Ancrenaz, I., Mohamed, M., Andau, P. y Bruford, M.W. (2005). Patterns of genetic diversity and migration in increasingly fragmented and declining orang‐utan (Pongo pygmaeus) populations from Sabah, Malaysia. Molecular Ecology, 14(2), 441-456 Grubb, P. (1990). Primate geography in the Afro-tropical rain forest biome. In G. Peters & R. Hutterer (Eds.), Vertebrates in the tropics Bonn: Alexander Koenig Zoological Research Institute and Zoological Museum Haffer, J. (1967). Speciation in Colombian forest birds west of the Andes. American Museum novitates, no. 2294. Harcourt, A. y Wood, M. (2012). Rivers as barriers to primate distributions in Africa. International Journal of Primatology, 33, 168–183. Jalil, M.F., Cable, J., Sinyor, J., Lackman-Ancrenaz, I., Ancrenaz M., Bruford, M.W. y Goossens, B. (2008). Riverine effects on mitochondrial structure of Bornean orang‐utans (Pongo pygmaeus) at two spatial scales. Molecular Ecology, 17(12), 2898-2909. Link, A., Valencia, L.M, Céspedes, L.N., Duque, L.D., Cadena, C.D. y Di Fiore, A. (2015). Phylogeography of the Critically Endangered Brown Spider Monkey (Ateles hybridus): Testing the riverine Barrier Hypothesis. International Journal of Primatology, 36(3), 530-547. Lynch-Alfaro, J.W., Boubli, J.P., Paim, F.P., Ribas, C.C., da Silva, M.N.F., Messias, M., Röhe, F., Mercês, M.P., Silva Jú nior, J.S., Silva, C.R., Pinho, G.M., Koshkarian, G., Nguyen, M.T.T., Harada, M.L., Rabelo, R.M., Queiroz, H.L., Alfaro, M.E. y Farias, I.P. (2015). Biogeography of squirrel monkeys (genus Saimiri): South-central Amazon origin and rapid pan-Amazonian diversification of a lowland primate. Molecular Phylogenetics and Evolution, 82, 436-454. Markolf, M. y Kappeler, P.M. (2013). Phylogeographic analysis of the true lemurs (genus Eulemur) underlines the role of river catchments for the evolution of micro-endemism in Madagascar. Frontiers in zoology, 10(1), 70. Mercês, M.P., Lynch-Alfaro, J.W., Ferreira, W.A.S., Harada, M.L. y Silva-Junior, J.S. (2015). Morphology and mitochondrial phylogenetics reveal that the Amazon River separates two eastern squirrel monkey species: Saimiri sciureus and S. collinsi. Moleculas Phylogenetics and Evolution, 82, 426–435. Moreno, N., Guzmán-Caro, D.C., Cortés-Rincón, J. y Henao-Díaz, F. (2017a). Mapa de distribución de Cheracebus lucifer en Colombia. En: www.asoprimatologicacolombiana.org. Asociación Primatológica Colombiana. Moreno, N., Guzmán-Caro, D.C., Cortés-Rincón, J. y Henao-Díaz, F. (2017b). Mapa de distribución de Cheracebus lugens en Colombia. En: www.asoprimatologicacolombiana.org. Asociación Primatológica Colombiana. Moritz, C., Patton, J.L., Schneider, C.J. and Smith, T.B. (2000). Diversification of rainforest faunas: an integrated molecular approach. Annual review of ecology and systematics, 31(1), 533-563. Muñoz‐Ortiz, A, Velásquez‐Álvarez, A.A, Guarnizo, C.E. y Crawford, A.J. (2015). Of peaks and valleys: testing the roles of orogeny and habitat heterogeneity in driving allopatry in mid‐elevation frogs (Aromobatidae: Rheobates) of the northern Andes. Journal of Biogeography, 42(1), 193-205. Olivieri, G., Zimmermann, E., Randrianambinina, B., Rasoloharijaona, S., Rakotondravony, D., Guschanski, K. y Radespiel, U. (2007). The ever-increasing diversity in mouse lemurs: three new species in north and northwestern Madagascar. Molecular phylogenetics and evolution, 43(1), 309-327. Peres, C.A, Patton, J.L. y da Silva, M.N.F. (1996). Riverine barriers and gene flow in Amazonian saddle-back tamarins. Folia Primatologica, 67(3): 113-124. Quemere, E., Crouau-Roy, B., Rabarivola, C., Louis Jr, E.E. y Chikhi, L. (2010). Landscape genetics of an endangered lemur (Propithecus tattersalli) within its entire fragmented range. Molecular Ecology, 19(8),1606-1621. Sandoval-H, J, Gómez, J.P. y Cadena, C.D. (2017). Is the largest river valley west of the Andes a driver of diversification in Neotropical lowland birds? The Auk: Ornithological Advances, 134(1), 168-180. Vences, M., Wollenberg, K.C. Vieites, D.R. y Lees, D.C. (2009). Madagascar as a model region of species diversification. Trends in ecology & evolution, 24(8), 456-465. Wallace, A.R. (1852a). Natural-History collectors in foreign countries. Zoologist, 10, 41-43. Wallace, A.R. (1852b). On the Monkeys of the Amazon. Proceedings of the Zoological Society of London, 20, 107-110. Wallace, A.R. (1898). The Wonderfull Century: Its Succeses and Its Failures. George N. Morang, Toronto, 400 pp. |
|
Asociación Primatológica Colombiana, APC
www.asoprimatologicacolombiana.org asoprimatologica@gmail.com Bogotá DC, Colombia |
Última actualización: Agosto del 2023
Proudly powered by Weebly



 Canal RSS
Canal RSS
